塩化水素の5つの特徴!高校化学の重要ポイント
塩化水素(HCl)について説明しましょう。
塩化水素はハロゲン化水素(ハロゲン化物イオンと水素イオンの化合物)のひとつです。
塩化水素の特徴は?
全部で5コ覚えておきましょう。
1.まず、常温・常圧での状態はなんでしょう?
気体ですね。
塩化水素の沸点は約-85℃でハロゲン化水素のなかで最も低い値を取ります。
ハロゲン化水素はどれも無色で刺激臭があり有毒な気体です。
2. 酸塩基で言うと何性ですか?強い?弱い?
強酸
このあたりまでは基本ですね~
3. 水には溶けやすい?
むちゃくちゃ溶けやすいです。
ハロゲン化水素は水H₂Oと同じく極性分子であるためよく溶けます。
その水溶液が『塩酸』で、液性は酸性を示します。
4. 検出方法は?
アンモニア水を近づけると、白煙が生じる。
NH3+HCl → NH4Cl
この反応を利用してアンモニアと塩化水素の両方の検出を行うことができます。
5. それじゃあ実験室での発生方法は?
HCl が欲しいんだから、H+とCl-をくっつければいいわけです。
まずはCl-から行きましょう。
Cl-はどこから持ってきましょう?
→身近なものでCl-が含まれているるものを考えましょう。
え~と、え~と (・´ω_,`・●)
はい、食塩の主成分であるNaClですね。
じゃあH+は?
Cl-とくっつけないといけないわけだから、強酸である必要がありますね。
強酸と言えば、
塩酸、硫酸、硝酸
の3つ
そのうち、塩酸は今欲しい塩化水素を水に溶かした水溶液なわけだから、これがあるんだったらいま作る必要もないわけです。
そうなると、残り2択ですね。
硫酸か硝酸
じゃあどっちでしょう?
ここで、カギとなるのが、「揮発性」です。
硫酸の揮発性は?
というと、濃硫酸は不揮発性です(希硫酸は揮発性ですが)。
硝酸は?
揮発性です。
ちなみに、塩酸は?
これは揮発性
ですので、不揮発性の濃硫酸がふさわしいですね!
え、なんで?(゚∇゚;)
というと、これはちと難しい話なんですが・・・(゚ー゚;
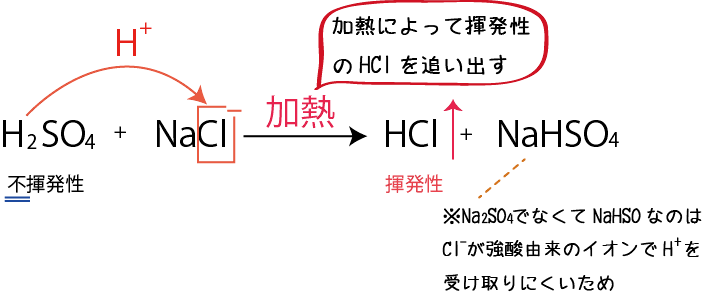
図を描いて説明しましょう。
という形で、加熱をすることで、揮発性のHClを追い出してるんですね。
このとき塩化水素は下方置換で回収します。
最後のHCl発生反応はちと難しかったですね~
☆化学のおすすめ参考書